Nghiên cứu chế tạo màng polymer trên cơ sở chitosan và poly(vinyl alcohol)
1. Đặt vấn đề
Ngày nay, an toàn thực phẩm luôn là một vấn đề nhận được sự quan tâm của các cơ quan chức năng quản lý nhà nước lẫn người dân. Việc sử dụng hóa chất để bảo quản thực phẩm như trái cây, rau quả, thịt cá… có thể giúp giữ tươi lâu hơn nhưng lại rất có hại cho sức khỏe của người tiêu dùng. Ngoài ra, người ta cũng sử dụng các vật liệu bao gói thực phẩm được làm từ màng nhựa như: polyethylene (PE), polypropylene (PP), polystylene (PS), Polyvinyle cloride (PVC)… Tuy nhiên, các vật liệu polymer tổng hợp này có một số hạn chế nhất định. Hàm lượng chất dinh dưỡng của thực phẩm được bảo quản bằng loại vật liệu này vẫn bị suy giảm trong quá trình bảo quản [1]. Hơn nữa, thời gian phân hủy chúng kéo dài, khó xử lý, gây ô nhiễm môi trường và có hại sức khỏe của con người.
Nhận ra được mặt trái của vần đề, con người bắt đầu nghĩ đến các loại vật liệu khác “thân thiện” hơn với môi trường. Đó là các sản phẩm mà sau khi sử dụng, chúng có thể tự phân hủy tạo ra các hợp chất đơn giản, có ích cho đất và đặc biệt không gây độc hại đến môi trường. Xuất phát từ nhu cầu thực tế đó, nghiên cứu chế tạo một loại màng bao thực phẩm có nguồn gốc tự nhiên, dễ bị phân hủy sinh học nhằm khắc phục những khuyết điểm của màng bao polymer hiện nay là cần thiết. Trong số những vật liệu đáp ứng cho nghiên cứu, chitosan là một vật liệu tiềm năng. Chitosan là một polisaccharide mạch thẳng. Nó có nguồn gốc từ các thành phần cấu trúc vỏ các loài giáp xác như tôm, cua… Hợp chất này có khả năng tương thích sinh học và tự phân hủy cao [13]. Nó không tan trong nước, có độc tính thấp, hoạt tính sinh học cao và đa dạng như kháng khuẩn, kháng nấm, tăng sinh tế bào, tăng cường khả năng miễn dịch, giảm cholesterol trong máu, hạn chế sự phát triển của khối u, có tác dụng nhanh trên các vết thương, vết bỏng [14]. Trong số các đặc tính đã nêu, hoạt tính kháng khuẩn của chitosan và các dẫn xuất của nó đối với cả vi khuẩn Gram âm [15] và Gram dương [16, 17] được xem là một trong các đặc tính quan trọng có liên quan trực tiếp đến tiềm năng ứng dụng sinh học của chúng trong việc tạo ra các chế phẩm bảo quản thực phẩm có nguồn gốc tự nhiên [18].
Tuy nhiên, màng làm từ chitosan giòn nên cần kết hợp với một polymer khác mềm dẻo hơn để tạo ra màng có độ mềm dẻo phù hợp. Poly(vinyl alcohol) (PVA) là một polymer tổng hợp nhưng có khả năng phân hủy sinh học. PVA không độc, có độ mềm dẻo cao và giá thành thấp. Do đó, việc phối hợp các polymer này lại sẽ tạo thành vật liệu tổ hợp được các ưu điểm của 2 polymer này. Chính vì vậy chúng có tìm năng thay thế các loại polymer tổng hợp không có khả năng phân hủy sinh học, đặc biệt là trong lĩnh vực bao bì thực phẩm. Đó là lí do thực hiện đề tài “Nghiên cứu chế tạo màng polymer trên cơ sở chitosan và poly(vinyl alcohol)”
2. Mục tiêu nghiên cứu: chế tạo màng từ chitosan và poly(vinyl alcohol) và xác định một số đặc tính của nó.
3. Đối tượng và phạm vi nghiên cứu:
3.1. Đối tượng nghiên cứu:
Màng polymer trên cơ sở chitosan và poly(vinyl alcohol)
3.2. Phạm vi nghiên cứu:
Nghiên cứu ảnh hưởng của hàm lượng chất đóng rắn, thời gian đóng rắn, nhiệt độ đóng rắn và thành phần chitosan/poly(vinyl alcohol) đến một số tính chất của màng như độ trương, độ thấm hơi nước, độ bền kéo, khả năng kháng khuẩn, nhiệt trọng lượng TGA…
4. Ý nghĩa khoa học và thực tiễn của đề tài
– Chitin là thành phần chính trong các phế thải của ngành công nghiệp chế biến thủy sản như nang mực, vỏ cua, tôm…nên việc tận dụng được thành phần này giúp nâng cao hiệu quả kinh tế, giảm ô nhiễm môi trường. Ngoài ra, mục tiêu xa hơn của đề tài là ứng dụng màng vào bảo quả rau quả sau thu hoạch, góp phần làm tăng giá trị các sản phẩm nông nghiệp của nước ta.
– Tăng cường khả năng kháng khuẩn khi bao gói, làm thời hạn bảo quản của sản phẩm dài hơn, đặc biệt trong ngành công nghệ thực phẩm.
– Giảm thực trạng ô nhiễm môi trường từ rác thải là các loại bao bì nhựa tổng hợp.
– Tăng hiệu quả kinh tế cho ngành công nghiệp Việt Nam.
CHƯƠNG 1 – TỔNG QUAN
1.1. Giới thiệu về polymer phân hủy sinh học
1.1.1. Khái niệm
Polymer phân hủy sinh học là loại vật liệu polymer mà quá trình phân hủy của nó do vi khuẩn đảm nhiệm, không đòi hỏi năng lượng, không tạo ra các chất độc hại cho môi trường.
1.1.2. Các loại polymer phân hủy sinh học
1.1.2.1. Các polymer phân hủy sinh học tự nhiên
Polysaccharide: tinh bột và cellulose, chitin và chitosan, Alginate, Gelatine.
1.1.2.2. Các polyester phân hủy sinh học
+ Polylactic acid: PLA
+ Polybutylene succinate: PBS
+ Polyester đồng trùng hợp mạch thẳng: AAC
+ Polybutyrate adipate terephthalate: PBAT
+ Polyhydroxyl butyrate: PHB
+ Polyhydroxyl valeate: PHV
+ Polycaprolactone: PCL
+ Polyethylene terephthalate: PET
+ Polyvilnyl alcohol: PVA
+ Ethylene vinyl alcohol: EVOH
1.1.3. Tình hình nghiên cứu trong nước và trên thế giới về các loại polymer phân hủy sinh học
1.1.3.1. Các nghiên cứu polymer sinh học trên thế giới
1.1.3.2. Các nghiên cứu polymer sinh học tại Việt Nam
1.1.4. Ứng dụng của polymer phân hủy sinh học
Các lĩnh vực ứng dụng cụ thể của polymer phân hủy sinh học:
1.1.4.1. Trong lâm, nông nghiệp
Polymer phân hủy sinh học được định hướng sử dụng để làm màng che phủ trong nông nghiệp nhờ khả năng tự phân hủy sau một thời gian nhất định dưới tác động của nhiệt độ, độ ẩm, ánh sáng và các vi sinh vật trong đất.
1.1.4.2. Ứng dụng làm bao bì, túi đựng hàng hóa
Polyme phân hủy sinh học được ứng dụng chủ yếu làm bao bì cho ngành công nghiệp thực phẩm. Để cải thiện tính chất của màng, người ta phối hợp polymer thiên nhiên và polymer tổng hợp.
1.1.4.3. Trong y học
Chất dẻo phân hủy sinh học được dùng làm vật liệu cấy trong phẫu thuật chỉnh hình và mạch máu, chỉ khâu phẩu thuật, ứng dụng trong chữa mắt….
1.2. Nguyên liệu chính sử dụng trong đề tài
1.2.1. Chitosan (CS)
1.2.1.1. Khái niệm
Chitosan là một trong số các polyme sinh học có nguồn gốc thiên nhiên. Chitosan là sản phẩm deaxetyl hoá của chitin có tên gọi là 2-amido-2-deoxy-D-gluco.
1.2.1.2. Cấu trúc của chitosan
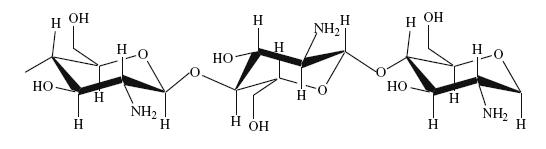 Chitosan một polysacarit mạch thẳng, là dẫn xuất đề axetyl hoá của chitin, trong đó nhóm (–NH2) thay thế nhóm (-NHCOCH3) ở vị trí C(2). Chitosan được cấu tạo từ các mắt xích D-glucozamin liên kết với nhau bởi các liên kết β -(1-4)-glicozit, do vậy chitosan có thể gọi là poly β -(1-4)-2-amino-2-deoxi-D-gluco hoặc là poly β -(1-4)-D- glucozamin
Chitosan một polysacarit mạch thẳng, là dẫn xuất đề axetyl hoá của chitin, trong đó nhóm (–NH2) thay thế nhóm (-NHCOCH3) ở vị trí C(2). Chitosan được cấu tạo từ các mắt xích D-glucozamin liên kết với nhau bởi các liên kết β -(1-4)-glicozit, do vậy chitosan có thể gọi là poly β -(1-4)-2-amino-2-deoxi-D-gluco hoặc là poly β -(1-4)-D- glucozamin

1.2.1.3. Tính chất hoá học của chitosan
a) Phản ứng ở nhóm hydroxyl
Tương tự như các ancol đa chức, tính axit của nhóm hydroxyl khá mạnh, chitin phản ứng được với Na, NaOH tạo thành hợp chất có cấu trúc ancolat gọi là chitin kiềm.
[C6H7O3NHCOCH3(OH)2]n+2nNaOH →[C6H7O3NHCOCH3(ONa)2]n + 2nH2O
Chitin kiềm là sản phẩm trung gian để sản xuất các chitin ete.
[Chit(ONa2)]n + 2nRX → [Chit(OR2)]n + 2nNaX
Phản ứng với axit, anhydric axetic hay HCl tạo ra sản phẩm ở dạng este. [Chit[OH)2]n + 2nHCl → [Chit(OCl)2]n + 2nH2O
b) Phản ứng ở nhóm axetamit
Chitin có khả năng tham gia phản ứng thể hiện tính chất amin bậc 2 như phản ứng đề axetyl hóa tạo thành chitosan.
Phản ứng trên thường được thực hiện trong dung dịch NaOH 40% ở 100-120°C, thời gian 1 đến 3 giờ. Hiệu suất phản ứng deaxetyl hóa đạt khoảng 70%. Do đó, sản phẩm phản ứng là mạch polyme chứa đồng thời các mắt xích N-axetyl-D-glucosamin đan xen với D-glucosamin.
c) Phản ứng ở nhóm amino
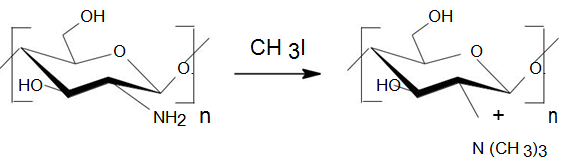
Dẫn xuất tan trong nước N,N,N-trimetyl chitosan đã được tổng hợp từ phản ứng của chitosan với CH3I với sự có mặt của NaI và N-metyl-2-pyrolidon/ NaOH.
d) Phản ứng cắt mạch polyme
Phản ứng cắt mạch có ý nghĩa quan trọng vì độ dài mạch quyết định trực tiếp đến các tính chất vật lý và hóa học của polyme. Chitin, chitosan là polyme có khối lượng phân tử lớn (10-500kDa) tùy thuộc vào nguồn gốc và phương pháp điều chế.
1.2.1.4. Ứng dụng của chitosan và dẫn xuất
Chitin, chitosan và các dẫn xuất của chúng có nhiều đặc tính quý báu như: có hoạt tính kháng nấm, kháng khuẩn, có khả năng tự phân huỷ sinh học cao, không gây dị ứng, không gây độc hại cho người và gia súc, có khả năng tạo phức với một số kim loại chuyển tiếp như: Cu(II), Ni(II), Co(II)…
Ứng dụng: Ứng dụng trong xử lý nước thải, y học, trong công nghiệp thực phẩm, nông nghiệp.
1.2.2 Poly(vinyl alcohol) (PVA)
1.2.2.1. Khái niệm
PVA là một polymer tan trong nước. PVA thu được bằng phản ứng thủy phân polyvinyl acetate.
1.2.2.2. Tính chất của PVA
a. Tính chất vật lý
Các tính chất quan trọng nhất là khả năng tan trong nước, dễ tạo màng, chịu dầu mỡ và dung môi, độ bền kéo cao, chất lượng kết dính tuỵêt vời và khả năng hoạt động như một tác nhân ổn định phân tán
b. Tính chất hóa học
Phản ứng ester hóa, phản ứng ether hóa, phản ứng acetal hóa
c. Sự phân hủy của PVA
PVA phân hủy sinh học cho hợp chất dioxide carbon và nước. Có khoảng 55 loài sinh vật khác nhau có khả năng phân hủy PVA
1.2.2.3. Ứng dụng của PVA
Keo dán, chất kết dính, hồ và phủ giấy, hồ sợi và hoàn thiện, tác nhân tạo mũ, màng PVA, gốm, các sản phẩm đúc.
1.2.2.4. Sản xuất PVA
Khi sản xuất PVA phải sử dụng phương pháp nhiều bước vì monomer vinyl alcohol là một thực thể không tồn tại, bản thân nó tự sắp xếp lại thành acetaldehid. Vì vậy, trước tiên cần phải tạo ra nhựa polyvinyl acetate, sau đó alcol phân polyvinyl acetate thành PVA.
1.2.3. Glutaraldehyde (GA)
1.2.3.1. Khái niệm
Glutaraldehyde là một loại chất khử trùng, cũng như là một loại dược phẩm. Nếu dùng với vai trò một chất khử trùng, GA có hiệu quả chống lại một loạt các vi sinh vật kể cả bào tử của chúng.
1.2.3.2. Vai trò
Glutaraldehyde là tác nhân đóng rắn của PVA. Khi phản ứng xảy ra, GA đóng vai trò là cầu nối ngang giữa 2 phân tử PVA, từ đó hình thành mạng lưới không gian trong sản phẩm đóng rắn, làm mất tính tan của sản phẩm.
1.2.3.3. Tính chất
| Tên hóa học | Glutarandehyde |
| Công thức phân tử | C5H8O2 |
| Công thức cấu tạo | OHC-CH2-CH2-CH2-CHO |
| Trạng thái | Lỏng |
| Mùi | Táo thối |
| Trọng lượng phân tử | 100.13 |
| Điểm sôi | 200.9oC |
| Tính ổn định và khả năng phản ứng | Không tưởng thích với các chất oxy hóa mạnh và bazơ mạnh |
| Độ hòa tan | Tan trong nước, rượu, ete và các dung môi tương tự |
1.2.3.4. Ứng dụng
Glutaraldehyde ứng dụng trong thương mại và công nghiệp rất đa dạng, bao gồm kiểm soát vi khuẩn bất lợi và độc hại trong các hệ thống mỏ, chất lỏng xử lý kim loại, giấy và bột giấy, vệ sinh an toàn vật nuôi và vệ sinh thiết bị y tế. Ngoài ra GA có thể được sử dụng như một loại chất bảo quản cho các sản phẩm tiêu dùng công nghiệp khác nhau, để bảo vệ chúng khỏi vi khuẩn và nấm mốc, qua đó kéo dài tuổi thọ của sản phẩm.
1.2.4. Acid acetic
1.2.4.1. Khái niệm
Acid acetic có công thức hóa học CH3COOH, là một chất lỏng không màu. Khi không pha loãng thì được gọi là acid acetic băng
1.2.4.2 Tính chất hóa lý của acid axetic
Acid acetic với công thức hóa học CH3COOH, khối lượng phân tử 60,5 kg/kmol, nhiệt độ nóng chảy tnc= 16,63oC, nhiệt độ sôi ts= 118oC, tỷ trọng 1,049, độ nhớt ở 20oC là 1,21.10-3 Ns/m2
1.2.4.3 Ứng dụng acid axetic
Acid acetic là loại acid vô cơ được ứng dụng rộng rãi trong đời sống và trong sản xuất công nghiệp. Những ứng dụng quang trọng nhất của acid acetic gồm:
Ứng dụng acid acetic trong chế biến mủ cao su
Ứng dụng acid acetic trong công nghệ thực phẩm
Ứng dụng acid acetic trong các ngành công nghiệp khác
CHƯƠNG 2- PHƯƠNG PHÁP NGHIÊN CỨU
VÀ THỰC NGHIỆM
2.1. Sơ đồ nghiên cứu:
– Bước1:
– Bước 2
– Thuyết minh sơ đồ:
Bước 1:
Các màng PVA được gia công với các hàm lượng acid acetic khác nhau. Hàm lượng GA so với PVA được cố định là 3/100 phần khối lượng. Các màng này sau đó được đóng rắn ở nhiệt độ và thời gian lần lượt là: 900C trong 3, 5, 7h và 1200C trong 1, 3, 5h. Sở dĩ lựa chọn thời gian đóng rắn như vậy nhằm mục đích rút ngắn thời gian đóng rắn và tăng năng suất.
Bước 2:
Tiến hành phối trộn 5%, 10% và 15% hàm lượng chitosan trong màng với PVA và các thành phần khác theo tỷ lệ tối ưu đã được tìm ra. Các mẫu được đóng rắn ở điều kiện tối ưu đã lựa chọn. Khảo sát các tính chất của màng: Độ trương, độ thấm hơi nước, độ bền kéo, khả năng kháng khuẩn, nhiệt trọng lượng TGA.
2.2 Thực nghiệm:
2.2.1 Hóa chất:
NaOH (rắn), Acid acetic (Dung dịch 50% trong nước), Chitin, Poly (vinyl alcohol) (độ thủy phân 99%), Glutaraldehyde (dung dịch 50% trong nước)
Máy khuấy từ, Tủ sấy, Đĩa petri, Cốc đựng thủy tinh, Đũa khuấy thủy tinh,Cân điện tử, Ống pipet, Hạt silicagen, Khuôn thuỷ tinh, Bình hút ẩm ….
2.2.3 Cách tiến hành:
a. Deacetyl hóa Chitin
Sử dụng 400g dung dịch NaOH 4M để deacetyl hóa 46g Chitin, khuấy trộn bằng máy khuấy từ và gia nhiệt ở 90 0C trong 4h. Sau đó đem lọc rửa chitosan thu được đến khi pH trung tính và sấy khô.

Hình 2.1: Chitosan đã được deacetyl hóa
Mức độ deacetyl hóa được xác định bằng phổ hồng ngoại biến đổi Fourier. Độ deacetyl hóa của sản phẩm là 52%. Chitosan thu được hòa tan trong dung dịch acid acetic 2% với nồng độ chitosan là 3%.
Hình 2.2: Phổ hồng ngoại của chitosan
Lượng PVA và nước cất được tính toán để tạo dung dịch 10% PVA được cho vào cốc thủy tinh có cánh khuấy từ. Tiến hành khuấy với tốc độ chậm ở nhiệt độ phòng trong 30 phút, sau đó vừa khuấy vừa gia nhiệt cho hỗn hợp lên 900C. Tiếp tục duy trì khuấy trộn ở nhiệt độ này cho đến khi PVA tan hoàn toàn trong nước tạo dung dịch trong suốt.
Màng polymer được ngâm trong nước sau một thời gian xác định, mẫu được lấy ra sau đó lau khô bề mặt bằng giấy thấm và cân. Độ trương của mẫu (Rs) được tính theo công thức sau:
Độ bền kéo của màng được đo tại phòng thí nghiệm Polymer trường Đại học Bách Khoa – Đại học Đà Nẵng theo tiêu chuẩn ASTM D638 với tốc độ kéo 50 mm/phút.
e. Xác định khả năng kháng khuẩn
Kiểm tra mức độ kháng khuẩn của các màng trên vi khuẩn Gram dương (Bacillus Subtilis). Chuẩn bị các màng PVA trắng, PVA đóng rắn bằng GA và màng trên cơ sở PVA và Chitosan. Bằng phương pháp đặt màng trong đĩa thạch đã cấy sẵn vi khuẩn, sau 12h kiểm tra tính chất này.
g. Xác định độ thấm hơi nước của màng
Độ thấm hơi nước (WVP) được xác định theo phương pháp ASTM E 95-96 (ASTM 1995b). Mẫu màng được cố định lên hộp nhôm có chứa sẵn silicagen bên trong để giữ độ ẩm ban đầu bên trong hộp là 0%. Sau đó đặt vào bình hút ẩm có điều chỉnh độ ẩm tương đối của môi trường trong bình 50±5% bằng dung dịch muối Mg(NO3)2 bão hòa.
f. Phân tích nhiệt trọng lượng TGA
Mẫu được đo TGA trên máy STA 6000 của Hãng PerkinElmer. Khối lượng mẫu sử dụng từ 3 đến 5 mg, môi trường ni tơ với lưu lượng 20 ml/phút, tốc độ gia nhiệt 10 oC/phút.
g. Khảo sát khả năng phân hủy sinh học
Mẫu được chôn trong đất ngoài môi trường tự nhiên và định kỳ được lấy lên để quan sát sự thay đổi ngoại quan.
CHƯƠNG 3- KẾT QUẢ NGHIÊN CỨU VÀ THẢO LUẬN
3.1. Kết quả nghiên cứu
Các nghiên cứu đóng rắn PVA bằng glutaraldehyde đã được thực hiện trong phạm vi nhiệt độ khá rộng, từ nhiệt độ thường [54] đến nhiệt độ khá cao, 70oC [55] . Các kết quả đều cho thấy dù ở nhiệt độ phòng hay nhiệt độ cao thì quá trình đóng rắn vẫn xảy ra, tuy nhiên thời gian đóng rắn sẽ thay đổi, nhiệt độ càng thấp thì thời gian đóng rắn càng dài. Điều này phù hợp với lý thuyết, khi nhiệt độ tăng và tốc độ phản ứng tăng và do đó rút ngắn thời gian đóng rắn. Với mong muốn có thể đóng rắn PVA trong thời gian ngắn nên đề tài chọn đóng rắn ở nhiệt độ cao.
Kết quả thu được thể hiện ở bảng 3.1: Kết quả khảo sát độ trương của màng PVA ở các hàm lượng acid acetic và thời gian, nhiệt độ đóng rắn khác nhau
3.1.1.1 Ảnh hưởng của hàm lượng acid acetic đến tính chất của màng
Hình 3.1: Biến thiên độ trương của màng ở các hàm lượng acid acetic khác nhau (sử dụng 3/100 (GA/PVA) phần khối lượng) với nhiệt độ đóng rắn ở 90oC trong 7h)
Độ trương của PVA đóng rắn với hàm lượng acid cao có thể do sự có mặt của acid acetic, một hợp chất ưa nước, trong sản phẩm làm tăng tính ưa nước của nó. Kết quả xác định sự biến thiên độ trương của màng ở các hàm lượng acid acetic khác nhau
a. Ảnh hưởng của thời gian và nhiệt độ đóng rắn đến tính chất của màng
Ở nhiệt độ đóng rắn 90oC, khi tăng thời gian đóng rắn thì độ trương giảm, chỉ trừ trường hợp mẫu mẫu có hàm lượng acid 9,5/100. Mẫu này có độ trương giảm khi tăng thời gian đóng rắn từ 3h lên 5h nhưng khi tăng thời gian đóng rắn lên 7h thì độ trương tăng lên.
Hình 3.2: Ảnh hưởng của thời gian đóng rắn đến độ trương của màng (sử dụng 3/100 GA và 3,5/100 acid acetic phần khối lượng so với PVA), đóng rắn ở 90 0C
 b. Ảnh hưởng của hàm lượng GA đến tính chất của màng
b. Ảnh hưởng của hàm lượng GA đến tính chất của màng
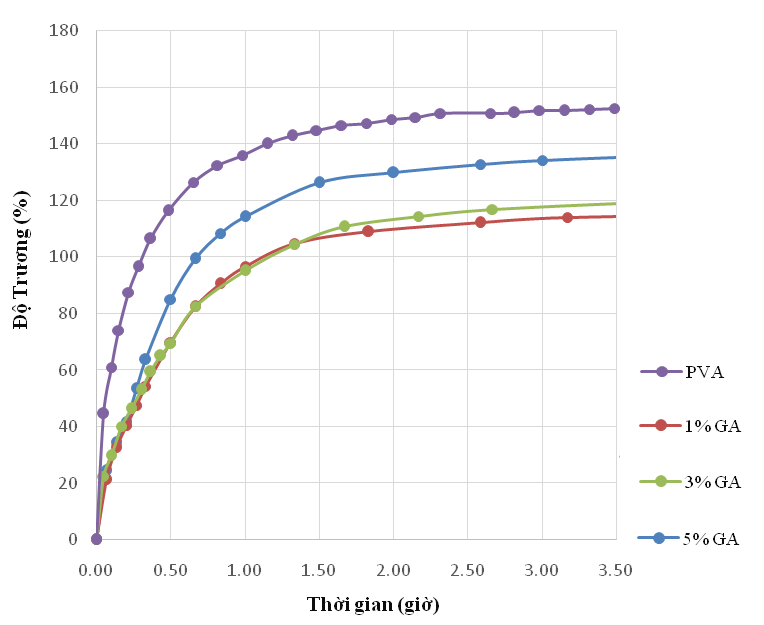
Hình 3.3: Ảnh hưởng của hàm lượng GA đến độ trương của màng PVA ở nhiệt độ đóng rắn 90 0C trong 7h
Khi tăng hàm lượng GA thì độ trương của sản phẩm thu được tăng theo. GA là tác nhân đóng rắn cho PVA. Khi phản ứng đóng rắn xảy ra, GA đóng vai trò là cầu nối ngang giữa 2 phân tử PVA, từ đó làm hình thành mạng lưới không gian trong sản phẩm đóng rắn, làm mất tính tan của sản phẩm.
Khi hàm lượng của GA thấp, liên kết ngang hình thành thưa thớt, chiều dài mạch PVA giữa 2 liên kết ngang lớn nên độ trương của PVA đóng rắn lớn. Tăng hàm lượng GA làm xuất hiện liên kết ngang dày đặc hơn
3.1.2 Ảnh hưởng của hàm lượng Chitosan đến tính chất cơ lí, khả năng kháng khuẩn và độ trương của màng.
3.1.2.1 Ảnh hưởng của hàm lượng chitosan đến độ trương của màng
Hình 3.4: Ảnh hưởng của hàm lượng chitosan đến độ trương của màng
Các màng phối hợp với CS được gia công ở hàm lượng GA bằng 1/100 phần khối lượng so với PVA, đóng rắn ở nhiệt độ 90oC trong thời gian 7h. Việc thêm chitosan vào trong thành phần nguyên liệu đã làm giảm rõ rệt độ trương trong nước của màng. Khi không có chitosan độ trương của màng là 121%, độ trương giảm xuống còn khoảng 70-80% khi hàm lượng chitosan trong màng thay đổi từ 5% đến 15%. Kết quả này có thể giải thích rằng do tính kị nước của chitosan mang lại. Kết quả thí nghiệm còn cho thấy độ trương không giảm nhiều khi tăng hàm lượng chitosan trong màng từ 5% lên 15%.
3.1.2.2 Ảnh hưởng của hàm lượng chitosan đến tính chất cơ lí của màng
Hình 3.5: Độ bền kéo của màng (N/mm2)
Độ bền kéo của màng khi phối hợp PVA/CS theo các tỉ lệ khác nhau được thể hiện ở hình 3.4. Ta thấy rằng các màng phối hợp với chitosan đều cho giá trị độ bền kéo cao hơn so với màng PVA khi chưa phối trộn với CS. Khi tăng dẫn hàm lượng chitosan độ bền màng tăng lên và sau đó giảm xuống. Màng chứa 10% CS có độ bề kéo cao nhất, cụ thể là 78 N/mm2, sau đó giảm còn 59.5 N/mm2 khi tăng hàm lượng CS lên 15%. Kết quả này phù hợp với nghiên cứu của Esam A. El-Hefian và các cộng sự [49].
3.1.2.3 Khả năng kháng khuẩn của màng
Khi đưa chitosan vào màng thì màng sẽ có khả năng kháng khuẩn gram dương. Có 2 cơ chế kháng khuẩn được đề nghị đối với chitosan. Cơ chế thứ nhất cho rằng khả năng chống vi khuẩn của chitosan xuất phát từ bản chất polycationic của nó. Khi có mặt acid, nhóm NH2 sẽ bị proton hóa, điện tích dương của nhóm amino sẽ tương tác với phần mang điện âm của màng tế bào vi khuẩn làm thay đổi tính chất barrier của chúng nên ngăn cản sự đi vào của dưỡng chất và/hoặc gây ra sự giảm nội bào. Cơ chế thứ 2 cho rằng sự kháng khuẩn có liên quan đến việc thấm chitosan KLPT thấp vào bên trong tế bào, liên kết với DNA và kết quả là ức chế sự tổng hợp RNA và protein
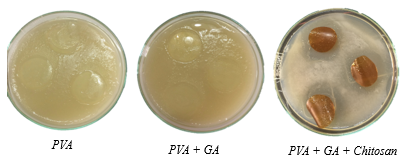
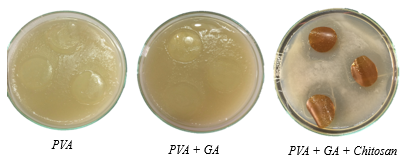
Hình 3.6: Khả năng kháng khuẩn của màng
3.1.3. Phân tích nhiệt trọng lượng TGA
Hình 3.7: TGA của các màng PVA
Đường cong TGA của chitosan cho thấy có sự giảm khối lượng (khoảng 12%), ở khoảng nhiệt độ nhỏ hơn 220 oC. Sự mất khối lượng ở giai đoạn này có thể do sự bay hơi của nước và các sản phẩm thấp phân tử tạo ra trong quá trình deacetyl hóa. Giai đoạn có tốc độ phân hủy lớn nhất là từ 220oC đến 300oC.
Với PVA quá trình phân hủy gồm 3 giai đoạn. Giai đoạn 1 ở khoảng nhiệt độ nhỏ hơn 230oC với sự mất khối lượng khoảng 3%, Giai đoạn 2 từ 230oC đến 340oC và giai đoạn 3 ở nhiệt độ trên 340oC.
Khi phối hợp chitosan vào PVA làm cho tốc độ phân hủy của giai đoạn 2 tăng lên, đồng thời Tmax giảm xuống so với trường hợp PVA đóng rắn, còn 280oC
Hình 3.8: DTG của các màng PVA và CS
3.1.4. Độ thấm hơi nước
Hình 3.9: Đồ thị biểu diễn độ tăng khối lượng (gam) của màng PVA theo thời gian (giờ)
Hình 3.10: Độ thấm hơi nước của màng
Các màng sử dụng đo độ thấm hơi nước có chiều dày trung bình 0,19 ± 0,04 mm. Từ kết quả đo sự thay đổi khối lượng cốc theo thời gian và diện tích màng tính được độ thấm hơi nước qua màng. Từ hình này cho thấy độ thấm hơi nước của màng PVA chứa 5 và 10 % chitosan tương tự màng PVA không đóng rắn và có đóng rắn. Tuy nhiên, khi tăng hàm lượng chitosan trong màng lên 15% thì độ thấm hơi nước giảm xuống.
3.1.5. Khả năng phân hủy sinh học
Mẫu sau khi chôn dưới đất ở độ sâu 20 cm trong 50 ngày. Nhìn bằng mắt thường thì chưa thấy sự thay đổi về ngoại quan mẫu. Tuy nhiên tất cả các mẫu đều đã có rể cây bám lên. Điều này chứng tỏ sự tương thích sinh học của các màng, đồng thời các màng cũng có thể là nơi cung cấp dưỡng chất hoặc nước cho thực vật. Sự bám rể cây lên màng có thể sẽ thúc đẩy sự phân hủy màng nhanh hơn.

Hình 3.11: Màng PVA không đóng rắn (a), PVA đóng rắn (b) và PVA có 15% chitosan (c) sau khi chôn trong đất trong 50 ngày
KẾT LUẬN VÀ KIẾN NGHỊ
Kết luận
Qua quá trình nghiên cứu, một số kết luận được rút ra như sau:
- Với PVA có khối lượng phân tử trung bình khối từ 85.000 đến 124.000 g/mol thì nồng độ dung dịch PVA tối đa có thể tạo màng bằng phương pháp đúc là 10%.
- Điều kiện tạo màng PVA đóng rắn tốt nhất là: GA/PVA = 1/100 phần khối lượng, Acid acetic/PVA = 3,5/100 phần khối lượng, thời gian đóng rắn là 7h và nhiệt độ đóng rắn là 90 phút.
- Phối hợp chitosan vào PVA sẽ làm giảm độ trương, tăng độ bền cơ lí và giúp cho màng có khả năng kháng khuẩn gram dương.
- Với hàm lượng chitosan nhỏ hơn 10% thì không ảnh hưởng đến độ thấm hơi nước của màng PVA, nhưng khi hàm lượng chitosan trong màng 15% thì độ thấm hơi nước của màng giảm xuống.
- Các màng đi từ PVA và chitosan cho thấy sự tương thích sinh học, đồng thời cũng có thể là nguồn cung cấp dưỡng chất cho thực vật.
Kiến nghị
- Tiếp tục theo dõi sự phân hủy sinh học của các mẫu đã được tổng hợp.
- Nghiên cứu ứng dụng màng để bảo quản một số thực phẩm.
- Khảo sát khả năng kháng khuẩn của màng PVA ở hàm lượng chitosan thấp hơn 5%.
- Khảo sát khả năng đóng rắn của màng PVA ở nhiệt độ phòng.
E:\DỮ LIỆU COP CỦA CHỊ YẾN\DAI HOC DA NANG\KY THUAT HOA HOC\KHOA 35\(R)9. Lam Thi Ni Na\13. Lam Thi Ni Na\TOM TAT





